Voordat we beginnen, eerst even een smaakmaker van waar we het over gaan hebben:
Video 1. Lichtflitsen uit Wint-O-Greenpepermuntjes van Life Savers.Voor de hele video, zie hier; video van YouTube-kanaal Smarter Every Day 2.
Wat je hierboven ziet is dat een alledaags pepermuntje spectaculaire natuurkunde kan vertonen. Eenzelfde fenomeen werd al opgemerkt door de wetenschapper Francis Bacon in 1605 [1], toen hij beschreef hoe suikerbrokken licht afgaven in het donker wanneer er suiker afgeschraapt werd. Waar we suiker tegenwoordig vooral kennen als een poeder van kleine kristallen, leidde het extractieproces van suiker uit bijvoorbeeld suikerriet in die tijd tot hele harde brokken die met de hand in kleinere stukjes gehakt of afgeschraapt moesten worden. Bacon zal dan ook niet de eerste zijn geweest die het daarbij vrijkomende licht heeft opgemerkt – iedereen die toendertijd in het donker suiker uit een houder probeerde te schrapen moet het licht ook hebben gezien. Met ons “moderne” suiker zou je dit effect overigens ook prima moeten kunnen zien!
Triboluminescentie
Waar komt dit suikerlicht vandaan? Het onderliggende fenomeen wordt triboluminescentie genoemd, wat afstamt van τρῑ́βω (“tribo”), het Griekse woord voor wrijven, en lumen, het Latijnse woord voor licht. Deze benaming is wat verwarrend, want het betreft hier bijvoorbeeld niet de opbouw van statische elektriciteit door middel van wrijving – het effect waardoor een ballon die je op je hoofd op en neer wrijft, naderhand je haar aantrekt. Wat de harde brokken suiker en het snoepje in de video doen oplichten, is het breken van het kristal.
Triboluminescentie blijkt overigens een heel normaal verschijnsel te zijn: ongeveer de helft van alle kristallen, materialen waarin de atomen in een herhalend patroon gerangschikt zijn, geven een vorm van licht af wanneer ze breken! [2] Natuurlijk is het wel zo dat niet alle kristallen evenveel licht afgeven, dus je kan het effect niet altijd even makkelijk waarnemen. Wat kristallen triboluminescent maakt, is dat ze piëzoelektrisch zijn. πιέζo, oftewel piëzo, is Grieks voor drukken of pletten; wanneer piëzoelektrische materialen geplet of uitgerekt worden, produceren ze een elektrisch veld. Dit werkt overigens ook andersom: als je een piëzoelektrisch materiaal in een elektrisch veld zet, veranderd de lengte ervan. Oom dit omgekeerde effect heeft veel toepassingen, maar daar hebben we het een andere keer over!
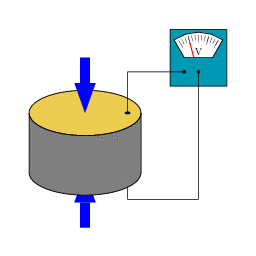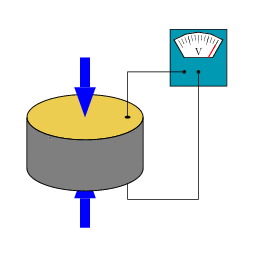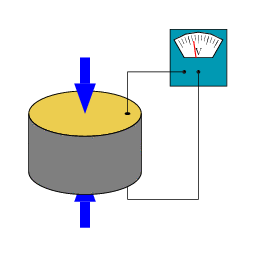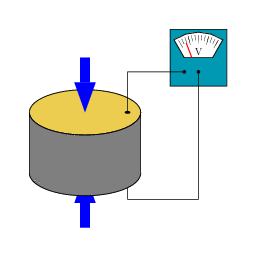
Afbeelding 2. Het piëzoelektrisch effectWanneer een piëzoelektrisch materiaal geplet wordt, ontstaat er een meetbaar ladingsverschil tussen de twee uiteinden ervan. Afbeelding: Wikipediagebruiker Tizeff
Uit het bovenstaande volgt ook dat niet alle kristallen licht geven wanneer ze breken: alleen kristalstructuren die geen inversiesymmetrie hebben kunnen piëzoelektrisch zijn. Wat betekent dat? Een kristal heeft inversiesymmetrie wanneer er in zijn kristalstructuur een punt bestaat van waaruit gezien voor alle atomen op posities (x,y,z) dezelfde soort atomen zich óók op locaties (-x,-y,-z) bevinden – zie afbeelding 3.
Wanneer zo’n inversiesymmetrie er niet is, bestaat er vrijwel altijd een klein netto elektrisch veld, een zogeheten dipoolmoment, in het kristalrooster. Als het rooster vervolgens geplet wordt, verplaatsten de atomen in de kristalstructuur zich en verandert daardoor ook de grootte van het interne elektrische veld. Zo zet het rooster de externe druk om in een ladingsverschil.

Afbeelding 3. Een piëzoelektrisch kristal.Dit materiaal, loodzirconaattitanaat, is een van de meest gebruikte piëzoelektrische materialen in industrie. Bij hoge temperaturen (links) is de structuur inversiesymmetrisch, met een inversiepunt (zwart) waar de stippellijnen elkaar kruisen. Als je het materiaal afkoelt tot onder een bepaalde temperatuur Tc wordt het kristalrooster verstoord en verliest het zijn inversiesymmetrie. Hierbij ontstaat er een klein ingebouwd ladingsverschil tussen de boven- en onderkant van het kristal (aangegeven door de pijl P), en wordt het materiaal piëzoelektrisch. Afbeelding: Wikipediagebruiker Pinin
En er was licht!
Laten we teruggaan naar de reden dat er bij het kapotslaan (of op een andere manier breken) van de pepermuntjes zoals in de video lichtflitsen te zien zijn. Als je een piëzoelektrisch materiaal breekt, zijn de nieuwe oppervlakken die ontstaan elektrisch geladen. Als het ladingsverschil tussen twee oppervlakten groot genoeg is, kunnen elektronen van de negatieve kant overspringen naar de positieve kant. Doen ze dit in lucht, dan is de kans groot dat deze elektronen eerst een luchtmolecuul tegenkomen voordat ze de (positief geladen) andere oppervlakte van het materiaal raken.
Door de energie van het elektron kan het luchtmolecuul in een aangeslagen toestand raken, waarin het bijvoorbeeld trilt. Om van die extra energie af te komen, zendt het molecuul lichtdeeltjes (fotonen) uit. Uit metingen van de lichtintensiteit per golflengte van het licht dat uitgezonden wordt door de Wint-O-Green pepermuntjes, blijkt dat het meeste uitgezonden licht afkomstig is van stikstofmoleculen (N2). [3] Dit is niet zo raar, want lucht bestaat voor meer dan 78% uit stikstof. Een kleiner deel van het licht dat de pepermuntjes produceren, wordt gemaakt door de smaakmaker methylsalicilaat, een soort olie waarvan de moleculen ook licht uitzenden door vanuit een aangeslagen toestand terug te vallen naar de grondtoestand, maar voor eenvoudigere kristallen zoals tafelsuiker speelt dat laatste effect geen grote rol.
De lichtflitsen uit Wint-O-Green pepermuntjes en tafelsuiker komen dus voornamelijk van het stikstof in de lucht. De kleur van het ontstane licht wordt dus niet direct door het materiaal zelf bepaald. Het is dus ook zo dat veel triboluminescente kristallen géén licht uitzenden wanneer ze niet in lucht maar in vacuüm opengebroken worden. Of, misschien nog leuker: je kunt zulke materialen ook openbreken in een houder gevuld met de gassen die ook in neon-verlichting gebruikt worden, zodat ze neon-kleuren uitzenden!

Afbeelding 4. Licht uit verschillende gassen.De buisjes die je ziet zijn gevuld met edelgassen, die door elektronen geioniseerd raken en daarmee in verschillende kleuren oplichten. Andere gassen dan edelgassen kunnen hier ook voor gebruikt worden: denk aan waterstof, deuterium, stikstof, zuurstof en zelfs kwik. Afbeelding: Wikipediagebruiker Alchemist-hp
Meer dan alleen kristallen
Hoewel we het in dit artikel alleen over kristallografische materialen hebben gehad, wordt triboluminescentie ook waargenomen in een heel ander materiaal: plakband! Dit kan je zelf uitproberen: trek in een donkere kamer een rol plakband open, en met een beetje geluk zie je hier wat lichtflitsen. Hoeveel licht er uitgezonden wordt verschilt per soort plakband, maar het verschijnsel is waargenomen bij diverse verschillende soorten tape. Ik heb het zelf geprobeerd met een normale rol plakband en een rol duct tape, en zag inderdaad licht, maar helaas te weinig om het met mijn telefooncamera te filmen. Hieronder een video van iemand die het wel is gelukt om dit verschijnsel vast te leggen:
Video 5. Plakband geeft ook licht!Video van YouTube-kanaal NurdRage. Een ander voorbeeld, waarin afplakband gebruikt wordt, vind je hier.
Bij plakband is geen sprake van een kristalstructuur, maar bij het lostrekken van plakband wordt het wel geladen, en vervolgens werkt het proces op dezelfde manier. Eenvoudig plakband blijkt nog zelfs nóg ineressanter te zijn: we zullen het in een volgend artikel hebben over hoe plakband precies plakt en ook hoe je er röntgenfoto’s mee kan maken!
Bronnen
[1] H. E. Newton. “A history of luminescence from the earliest times until 1900.” American Physical Society, 1959.
[2] A. J. Watson. “Triboluminescence.” Advances in Physics 26:6, 887-948, 1977.
[3] R. Angelos, J. I. Zink & G. E. Hardy. “Triboluminescence spectroscopy of common candies.” Journal of Chemical Education 56:6, 413-414, 1979.